科伦药业复方氨基酸(15)双肽(2)注射液过评 创新药获批临床
- 2022-02-23 18:00:09 健康一线
- 健康
2月21日,国家药监局官网显示,四川科伦药业的复方氨基酸(15)双肽(2)注射液以补充申请获批过评,是该产品首家过评企业。2月22日,科伦药业发布公告称,公司控股子公司四川科伦博泰生物医药与和铂医药共同开发的1类创新药SKB378/HBM9378注射液获批临床,同意该药品开展中重度哮喘适应症的临床试验。在此之前,四川科伦药业的口服降糖药利格列汀片以仿制4类报产获批,视同过评。
2022年02月21日药品批准证明文件待领取信息发布
复方氨基酸(15)双肽(2)注射液适用于不能口服或经肠道补给营养,以及通过这些途径补充营养不能满足需要的患者,尤其适用于中度至重度分解代谢状况的患者。
近年中国公立医疗机构终端复方氨基酸(15)双肽(2)注射液销售情况(单位:亿元)
来源:米内网中国公立医疗机构终端竞争格局
米内网数据显示,2020年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端复方氨基酸(15)双肽(2)注射液销售额近5亿元,2021年上半年同比增长超过10%,四川科伦药业市场份额最大,超过80%。
复方氨基酸(15)双肽(2)注射液有4家企业拥有生产批文,目前,仅有四川科伦药业一家过评,天津金耀集团湖北天药药业以仿制4类提交上市申请在审评审批中,获批后将视同过评。
药品基本情况
SKB378/HBM9378注射液是四川科伦博泰生物医药与和铂医药利用和铂医药技术平台H2L2全人源小鼠共同研发,具有全球知识产权的1类创新药,靶向TSLP(thymic stromal lymphopoietin,胸腺基质淋巴细胞生成素) 的全人源单克隆抗体,双方确定由四川科伦博泰生物医药与和铂医药(上海)作为申办方推进临床研究。
截至目前,全球范围内同靶点单克隆抗体研发进度最领先的为阿斯利康/安进的 Tezepelumab,该单抗2021年12月17日在美国获批上市,在中国正在进行III期临床试验。国内康诺亚、恒瑞等药企均在该靶点有布局,目前尚无同类产品在国内获批上市。
本文地址:http://www.cnzhilian.com/jiankang/2022-02-23/572035.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 上一篇:恒瑞迎劲敌!新时代药业吸入用七氟烷报产获受理
- 下一篇:华森制药证券事务代表葛磊辞职
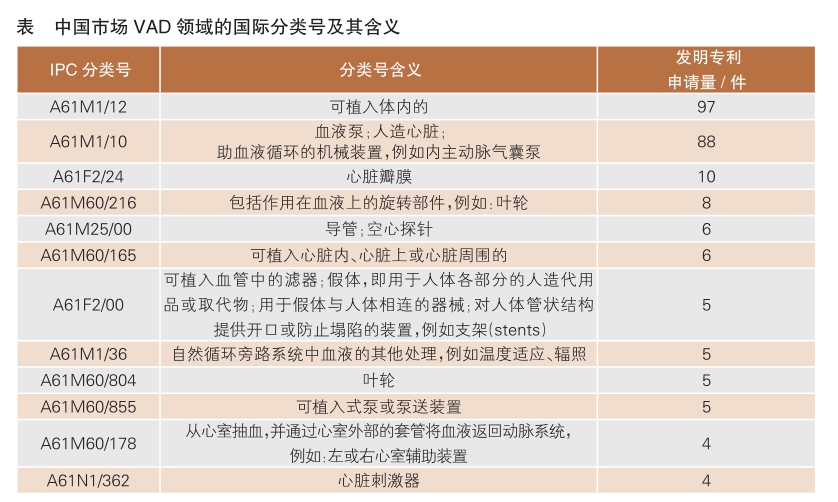
- 全球植入式心室辅助装置领域专利发展态势2022-02-23 18:01:34
- 【医疗器械知识知多少】医用诊察和监护器械(一)2022-02-23 18:01:17
- 基因编辑技术及相关IVD产品简述2022-02-23 18:01:06
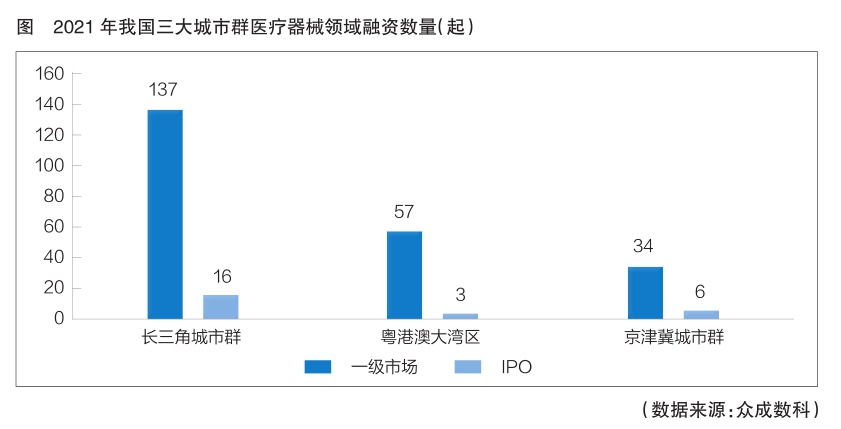
- 资源优化整合 资本市场活跃2022-02-23 18:00:41
- 187个产品获批注册 ——2021年11月批准注册医疗器械产品目录一览2022-02-23 18:00:20
-

 什么是阴痛?
什么是阴痛?
2021-10-26
-

 美立方国内外专家齐聚 颌面专家团再升级
美立方国内外专家齐聚 颌面专家团再升级
2021-08-23
-
《热点聚焦》医疗机构内新冠病毒感染防控有了新要求
2021-09-15 20:00:10
-
浙大一院2021年中秋节、国庆节放假及工作安排
2021-09-12 14:00:03
-
什么是阴结?
2021-10-26 10:33:42
-
名医风采 美立方颌面国际专家团,轮廓改造天团
2021-08-23 11:48:32
-
12333异地就医备案 您关心的都在这里
2021-09-07 10:40:49